Studien - IRIS-Studie  IRIS Immediate
Riskstratification Improves Survival
IRIS Immediate
Riskstratification Improves Survival
Gemeinsame Studie
Deutscher Kardiologischer Universitõtskliniken und der
Arbeitsgemeinschaft der Leitenden Kardiologischen Krankenhausõrzte (ALKK)
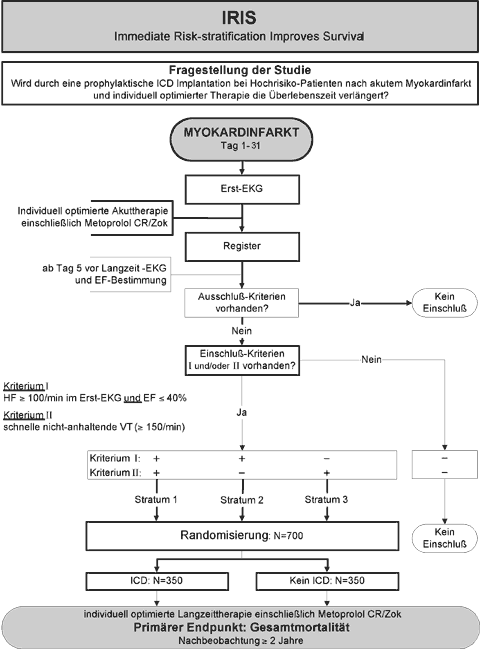
1. Fragestellung
Wird durch die prophylaktische ICD Implantation bei Hochrisikopatienten
nach akutem Myokardinfarkt [Tag 5-31] die Gesamtmortalitõt gesenkt?
2. Studienbegr³ndung und Design
Von den nach einem akuten Myokardinfarkt entlassenen Patienten versterben
in den folgenden 2 Jahren ca. 10% einen pl÷tzlichen Herztod [1, 2, 19,
33]. In mehreren Studien wurde durch eine gezielte Therapie mit Klasse I/III-Antiarrhythmika
die Prognose nicht verbessert [3, 7, 18, 37, 38]. Andererseits hat sich der
ICD in der Sekundõrprõvention bei Patienten mit Zustand nach Herz-
Kreislaufstillstand gegen³ber einer medikament÷sen Therapie als ³berlegen
herausgestellt [33]. Es stellt sich die Frage, ob der ICD bei Hochrisikopatienten
nach akutem Myokardinfarkt auch in der Primõrprõvention wirksam ist.
Die IRIS-Studie (Immediate Riskstratification
Improves Survival) ist eine multizentrische, offene randomisierte Studie mit
einer voraussichtlichen Patientenrekrutierungsdauer von 2,5 Jahren. Die Studie
pr³ft die Fragestellung, ob Patienten, die in der fr³hen Postinfarktphase
mittels nichtinvasiver Methoden als Hochrisikopatienten definiert wurden, von
einer Primõrprõvention durch einen ICD profitieren. Dabei wird auf
eine individuelle Optimierung der Infarkttherapie einschlie▀lich Beta-Blocker
Wert gelegt [21, 33, 39]. In dieser Studie soll Metoprolol CR/Zok, eingesetzt
werden.
Zur fr³hen Risikostratifikation der f³r
die IRIS-Studie in Frage kommenden Patienten werden ausschlie▀lich nichtinvasive
Methoden, die in allen Krankenhõusern mit Herzinfarktpatienten verf³gbar
sind, eingesetzt:
1. Ruhe-EKG (zur Bestimmung der Herzfrequenz zum
Zeitpunkt der stationõren Aufnahme)
2. Echokardiographie (zur Bestimmung der linksventrikulõren Ejektionsfraktion)
3. Langzeit-EKG (zur Dokumentation nichtanhaltender Kammertachykardien (VT)
Ad 1) Herzfrequenz im Erst-EKG
Ad 2) Linksventrikulõre Ejektionsfraktion (EF)
Ad 3) Nichtanhaltende Kammertachykardie
2.1 Einschlu▀kriterien
Patienten, die einen akuten transmuralen Myokardinfarkt ³berlebt haben
und mindestens eines der beiden folgenden Risiko-Kriterien erf³llen, werden
randomisiert mit einem ICD versorgt.
Ę Kriterium I:
Kombination von Herzfrequenz im Erst-EKG >100/min. [Tag 1-2]
und Ejektionsfraktion <40% [Tag 5-31]
und/oder
Ę Kriterium II:
Nichtanhaltende VT im Langzeit-EKG mit einer Frequenz >150/min. [Tag
5-31]
2.2 Ausschlu▀kriterien
Ausschlu▀kriterien: a) Patienten j³nger als 18 oder õlter
als 80 Jahre
b) Patienten mit klinisch therapiebed³rftigen Kammerarrhythmien vor dem
Indexinfarkt oder mehr als 48 Std. danach
c) Patienten mit therapierefraktõrer Herzinsuffizienz (NYHA IV)
d) Myokardinfarkt õlter als 31 Tage
e) Erst-EKG in Ruhe liegt nicht vor oder wurde spõter als 24 Stunden nach
Schmerzbeginn aufgezeichnet
f) Patienten mit Indikation zur ACB-Operation vor Einschlu▀
g) Patienten mit hirnorganischem Psychosyndrom
h) Zweiterkrankungen, die die Lebenserwartung deutlich limitieren
i) Patienten mit rechtsseitiger k³nstlicher Herzklappe
j) Patienten mit schlechter Compliance
k) Patienten, die an einer anderen Studie teilnehmen
l) Instabiler klinischer Zustand
m) Schwangerschaft
n) Nichteinwilligung des Patienten
2.2.1 Primõrer Endpunkt
Gesamtmortalitõt
2.2.2 Sekundõre Zielparameter
- Todesarten: pl÷tzlicher Herztod, nicht-pl÷tzlicher Herztod,
nicht-kardialer Tod
- Arrhythmische Ereignisse: Kammerflimmern, erfolgreiche Reanimation, symptomatische
anhaltende VT (> 30 Sekunden)
- Adõquate ICD-Interventionen: ICD-Schock und antitachykarde Stimulation
- Schwerwiegende kardiale und zerebrale Ereignisse: Rezidivinfarkt, PTCA, ACB-Operation,
Apoplex
- ICD-assoziierte Komplikationen
- Krankenhauseinweisungen jeglicher Ursache, durchgef³hrte Interventionen
und Kostenerfassung
- Lebensqualitõt
3. Studie in der ▄bersicht
3.1 Definition Akuter transmuraler Myokardinfarkt
In die IRIS Studie werden nur Patienten mit transmuralem Myokardinfarkt
(<31 Tage) eingeschlossen, wenn alle drei der folgenden Kriterien erf³llt
sind:
1. Brustschmerz: >20 Minuten oder Symptomõquivalent
2. EKG: > 0.1 mV ST-Hebung in zwei benachbarten Extremitõtenableitungen,
und/oder
> 0.2 mV ST-Hebung in zwei benachbarten Brustwandableitungen, oder
neu aufgetretener Linksschenkelblock, oder
neu aufgetretene Q-Zacke (> 0,03 s)
3. Enzyme: Erh÷hung der CK > dem 2-fachen des oberen Normwertes und
CK-MB > 6% mit Troponin
3.2 Studienzentren
An dieser Studie nehmen Zentren teil, die fundierte Erfahrung in der Betreuung
von Infarktpatienten haben (zuweisende Zentren) oder die selbstõndig ICDs
implantieren (Implantationszentren). Geographisch sind diese Zentren ³ber
ganz Deutschland verteilt.
3.2.1 ICD - Gerõtebeschreibung
Es werden CE-zertifizierte Einkammer ICD-Modelle der Firma Medtronic seit
dem Micro JewelÖ II, Modell 7223Cx oder neueren Zulassungsdatums eingesetzt.
Alle Produkte besitzen die Active CanÖ-Technologie und sind zur pektoralen
Implantation geeignet.
Das Medtronic Modell 7223 Cx, Micro JewelÖ
II, hat ein Volumen von 54 ccm, ein Gewicht von 97g, eine Speicherkapazitõt
von 128 kB und gewõhrleistet eine maximale Energieabgabe von 30 Joule.
Das Gerõt erm÷glicht eine detaillierte Analyse aufgetretener und detektierter
tachykarder Herzrhythmusst÷rungen, was f³r die Beurteilung eines effektiven
Patientenmanagements notwendig ist. Das PCDÖ System Micro JewelÖ II
verf³gt zur Erh÷hung der Erkennungsspezifitõt und damit zur Vermeidung
inadõquater Therapieabgaben ³ber fortschrittliche Algorithmen wie
z.B. das Onset-, Stabilitõts- und QRS-Breitenkriterium.
In seltenen Fõllen k÷nnen Patienten eine allgemein anerkannte Indikation
f³r einen Zweikammer-Schrittmacher aufweisen (siehe neue Richtlinien der
AHA). Ist dieser Patient f³r die ICD Gruppe randomisiert worden, erhõlt
er einen Zweikammer-ICD mit der M÷glichkeit der DDDR Stimulation (GEM DR,
Modell 7271, oder ein vergleichbares Nachfolgemodell).
Es wird versichert, da▀ alle implantierenden
─rzte eine detaillierte Einweisung der ICD-Gerõte erhalten haben,
die im Rahmen dieser Studie verwendet werden.
Principal Investigators
Prof. D. Andresen, Urban Krankenhaus Berlin
Prof. J. Senges, Herzzentrum Ludwigshafen
Prof. G. Steinbeck, Klinikum Gro▀hadern der LMU M³nchen
Co-Investigators
Dipl.-Ing. T. Br³ggemann, Urban Krankenhaus Berlin
PD Dr. E. Hoffmann, Klinikum Gro▀hadern der LMU M³nchen
Dr. K. Seidl, Herzzentrum Ludwigshafen
Biometrie
OSE Oncology Services Europe, M³nchen
Technische und finanzielle Unterst³tzung
Medtronic Bakken Research Center, Maastricht (NL)
Astra GmbH, Mitglied der AstraZeneca-Gruppe, Wedel
Hier k÷nnen Sie weitere Information und Unterlagen
zur Studie bestellen:
Ā
|